

NEWS CENTER
新闻中心
2019遗传毒性杂质控制指导原则审核稿
来源:英格尔医药科技中心 发布时间:2019-08-23
遗传毒性杂质控制指导原则(第一次征求意见稿)
遗传毒性杂质控制指导原则用于指导药物遗传毒性杂质的危害评估、分类、定性和限值制定,以控制药物中遗传毒性杂质潜在的致癌风险。为药品标准制修订,上市药品安全性再评价提供参考。
一、总则
遗传毒性(Genotoxcity)是指遗传物质中任何有害变化引起的毒性,而不考虑诱发该变化的机制,又称为基因毒性。遗传毒性杂质(GenotoxicImpurities,GTIs)是指能引起遗传毒性的杂质,包括致突变性杂质和其它类型的无致突变性杂质。其主要来源于原料药的生产过程,如起始原料、反应物、催化剂、试剂、溶剂、中间体、副产物、降解产物等。致突变性杂质(MutagenicImpurities)指在较低水平时也有可能直接引起DNA损伤,导致DNA突变,从而可能引发癌症的遗传毒性杂质。
本指导原则主要关注致突变机制的遗传毒性杂质,非致突变机制的遗传毒性杂质在杂质水平的剂量下,一般可忽略其致癌风险。
药品生产、药品标准提高及上市药品再评价过程中发现杂质后,可按本指导原则进行风险评估,确定其是否为遗传毒性杂质,尤其是致突变性杂质。如果一个杂质被鉴定为具有潜在的致癌风险,应制定相应的限值。在制订可忽略致癌风险的杂质限值时,应进一步分析生产工艺,兼顾安全性和质量风险管理成本两方面的因素,综合考虑制定合适的限值。
本指导原则包括危害评估方法、可接受摄入量计算方法和限值制定方法。
本指导原则中描述的对杂质潜在致突变性的评估方法不适用于以下类型的原料药和制剂:生物/生物技术制品、肽类、寡核苷酸、放射性药物、发酵产品、中药和动物或植物来源的粗制品。也不适用于已上市药物中使用的辅料、调味剂、着色剂和香料,以及与药物包材相关的可浸出物。
本指导原则中对杂质潜在致突变性的评估方法不适用于用于晚期癌症适应症的原料药和制剂,以及用于其它适应症但本身在治疗剂量下就具有遗传毒性,且预计可能与癌症风险增加有关的原料药。在这些情况下,致突变性杂质不会显著增加原料药的致癌风险。因此,杂质可以按非致突变性杂质的水平控制。
二、危害评估方法
遗传毒性杂质的危害评估方法主要是通过数据库、文献检索,(定量)构效关系((Quantitative)Structure-ActivityRelationships,(Q)SAR)评估以及遗传毒性试验等评估方法将杂质分类,参考国际相关分类方法,根据致突变和致癌风险危害程度可将杂质分为以下5类:
1类杂质指已知有致突变性的致癌物质。
2类杂质指致癌性未知的已知致突变性物质。
3类杂质指含有警示结构,与原料药结构无关,无致突变性数据的物质。
4类杂质指含有警示结构,与原料药或与原料药相关的物质具有相同的警
示结构的物质,且原料药或与原料药相关的物质经测试为无致突变性的物质。
5类杂质指无警示结构,或有充分的数据证明警示结构无致突变性或致癌性的物质。
1.数据库、文献检索评估方法
已有资料显示杂质是有致突变性的致癌物质,则将其归为1类;已有资料显示杂质是有致突变性,即细菌回复突变试验呈阳性,或有其它与DNA反应性相关的基因突变的阳性致突变性数据(例如,体内基因突变研究显示阳性),但无啮齿动物致癌性数据的物质,则将其归为2类;已有资料显示无致突变性或致癌性数据的物质,则将其归为5类。
2.(定量)构效关系((Q)SAR)评估方法
(Q)SAR评估方法是根据化合物警示结构和对细菌回复突变试验的预测对化合物进行分类。如果杂质含有与原料药结构无关的警示结构,但无致突变性数据,则可归为3类;如果杂质含有与原料药或与原料药相关的物质相同的警示结构(例如,工艺中间体),且该原料药或与原料药相关的物质经测试为无致突变性,则可归为4类;如果杂质含有警示结构,但有充分的数据认为该警示结构无致突变性或致癌性,或者杂质不含有警示结构,则可归为5类。
应用(Q)SAR方法进行计算机模拟,预测细菌回复突变试验的结果时,应采用两个互补的(Q)SAR预测方法。一个方法基于专家规则,另一个方法基于统计学。如果两个互补的(Q)SAR方法预测结果均没有警示结构,则可以认为该杂质没有致突变性,不建议做进一步的检测。
3.遗传毒性试验评估方法
对于应用(Q)SAR方法评估归为3类的杂质,可以进一步开展细菌回复突变试验。如果试验结果为阳性,则该杂质可以归为2类;如果试验结果为阴性,则该杂质可以归为5类。对于长期给药时杂质日摄入量超出1mg时,按照本指导原则评价为阴性的杂质,包括两个互补的(Q)SAR方法预测为阴性、或者细菌回复突变试验为阴性的,仍应考虑按照ICHQ3A/Q3B的要求对杂质进行潜在的遗传毒性评估,推荐的评估方法为体外点突变试验和体外染色体畸变试验。
对于致突变性(如细菌回复突变试验)结果为阳性的杂质,如果无法控制在可接受的摄入量,可以根据其作用机制和预期的靶器官(组织)分布,选择合适体内基因突变试验,如微核试验、Pig-a试验等,以明确其体内致突变风险,指导对其设定特定的限度。
三、遗传毒性杂质可接受摄入量的计算
确定遗传毒性杂质限值时主要的参考依据是每日可接受摄入量,每日可接受摄入量的计算方法包括:根据化合物特异性风险评估计算、根据毒理学关注阈值计算和根据给药周期调整计算等。
1.根据化合物特异性风险评估计算的可接受摄入量
具有阳性致癌性数据的致突变性杂质如果杂质具备足够的致癌性数据,则应采用化合物特异性风险评估方法来推导可接受摄入量,即根据导致50%肿瘤发生率的给药剂量(MedianToxicDose,TD50)线性外推法来计算化合物特异性的可接受摄入量,或使用国内外权威机构已公布的可接受摄入量参考值。
TD50线性外推法即通过啮齿类动物致癌性数据来计算杂质的可接受摄入量。如采用TD50值的1/50000作为摄入量,即相当于终生潜在发生肿瘤的风险为十万分之一。
每日可接受摄入量(AcceptanleDailyIntake,ADI)=TD50/50000×50kg
有实际阈值数据的致突变性杂质一些杂质的毒性对剂量的反应呈非线性或有实际阈值,针对此类杂质可通过未观察到作用剂量(NoObservedEffectLevel,NOEL)或者观察到作用的最低水平(Lowest-ObservedEffectLevel,LOEL)和采用不确定性因子来计算每日允许暴露量(PermittedDailyExposure,PDE)。
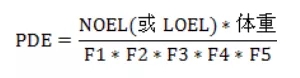
F1代表从不同物种外推到人的因子;F2为个体差异因子;F3为根据毒性暴露周期采用的可变因子;F4根据毒性严重情况采用的可变因子;F5在公式采用NOEL时一般为1,采用LOEL时根据毒性的严重程度,F5可以使用高达10的因子。
2.根据毒理学关注阈值(ThresholdofToxicologicalConcern,TTC)计算的可接受摄入量
单个杂质对于无毒理学研究数据的杂质可采用TTC计算可接受摄入量,即一个杂质的可接受摄入量为1.5µg/天。TTC是从TD50的剂量简单线性外推到十万分之一肿瘤发生率的剂量,且采用的TD50数据来自于最敏感物种和肿瘤发生的最敏感部位。在使用TTC作为评估原料药和制剂中致突变性杂质的可接受摄入量时,其对应的理论上终生患癌风险为十万分之一。TTC可以通用于大部分药物,作为可接受摄入量的默认值。
多个杂质根据TTC计算的可接受摄入量是针对单个杂质制定的。对于临床研发和已上市的药品,如果有3个或更多的2类或3类杂质,则可按多个杂质的总可接受摄入量,即5µg/天计算;如果原料药质量标准中有两个2类或3类杂质,应制定各自可接受摄入量;1类杂质应单独控制,不应计入2类和3类杂质的总可接受摄入量;另外,制剂中形成的降解产物应单独控制,不应计入总可接受摄入量。对于复方制剂杂质可接受摄入量制定,每种活性成分应单独规定。
3根据给药周期调整计算的可接受摄入量
已知致癌物的标准风险评估是假定癌症风险随着给药量的增加而增加,因此,终生以低剂量持续给药的致癌风险与相同的累积剂量平均分配在较短给药时长内的致癌风险等同。对于临床研发阶段和已上市药物已经可以预知该药物的给药时间,一般都是短于终生给药,所以可以调整上述计算的可接受摄入量,允许药物中致突变杂质的日摄入量高于终生给药时的值。
根据给药周期调整TTC的值1.5µg/天的摄入量一般用于终生长期治疗用(>10年)药物中存在的且无致癌数据的致突变杂质控制。短于终生给药的药品中致突变杂质摄入量可以调整为短期可接受更高的剂量,可理解为终生长期治疗用(>10年)药物中可接受的累积终生剂量(1.5μg/天×25550天=38.3mg)在短于终生给药期间平均分配在总给药天数中。
表1是从上述概念推导而得的数据,对于临床研发阶段和上市阶段药物,根据给药周期调整,给出了单个和多个杂质的可接受摄入量。因此应根据药物的实际给药时间计算杂质的可接受摄入量。间歇给药时,每日可接受摄入量应根据给药总天数计算,而不是给药的时间间隔。例如,2年期间每周服用一次的药物(即给药104天),其可接受摄入剂量为20μg/天。
表1:杂质的可接受摄入量
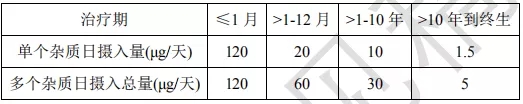
根据给药周期调整化合物特异性风险评估的值根据化合物特异性风险评估方法所推导的可接受摄入量也可以按表1以相同比例进行调整,或是根据日最大给药剂量限制在不超过0.5%,二者取较低者。例如,如果终生给药时根据化合物特异性风险评估方法所推导的可接受摄入量为15μg/天,用药周期短于终生给药时的限值(按表1比例),则可以增加至100μg/天(>1-10年治疗时长),200μg/天(>1-12个月)或1200μg/天(<1个月)。但是,对于一个具有最大日服用剂量的药物,例如,100mg,则<1个月时长的每日可接受摄入量应限制在0.5%(500μg),而不是1200μg。
本指导原则中描述的对杂质潜在致突变性的评估方法可用于所有给药途径,且一般不需要对可接受摄入量进行修正。由于所采用的评估方法较为保守,因此上述这些方法适用于所有患者人群。
四、遗传毒性杂质限值制定
在药品生产、药品标准提高及上市药品再评价过程中发现杂质后,首先通过上述风险评估方法将杂质分为1类、2类、3类、4类或5类。其次根据上述计算方法得到的杂质可接受摄入量,结合生产工艺,检测方法,临床使用情况等制定合适的限值。杂质限值一般按下式计算:

其中,杂质每日可接受摄入量即上文中ADI、PDE、TTC等数值。
1类杂质由于具有阳性致癌数据,应根据化合物特异性风险评估方法来推导可接受摄入量,此摄入量是基于终生的暴露量,再结合使用期限和其它因素制定合适的限值。
例1TD50线性外推法
某A药中含1类杂质a,A药推荐剂量为80mg/day,根据临床疗效可增加至160mg/day,最大剂量可为320mg/day。杂质在TOXNET数据库查得致癌相关数据:大鼠TD50为0.0959mg/kg/day,小鼠TD50为0.189mg/kg/day,在计算限值时,采用TD50较低即较为保守的值,即大鼠TD50值进行计算。
根据ADI=TD50/50000×50kg
则杂质a的每日最大摄入量为:
0.0959mg/kg/day÷50000×50kg=0.0959μg/kg/day
A药的每日最大临床剂量为320mg,则杂质a的限值为0.0959μg÷320mg=0.0003μg/mg=0.3ppm
例2通过NOEL值计算PDE
某B药中含1类杂质b,B药临床剂量为300mg/day。杂质b的小鼠NOEL
值为15.7mg/kg/day,则根据公式计算如下:

在本例中,
F1=12,考虑从小鼠外推到人
F2=10,考虑人的个体差异
F3=5,考虑研究的持续时间只有13周
F4=1,考虑未发现严重毒性
F5=1,考虑已测得无反应水平
B药的每日最大临床剂量为300mg/day,则杂质b的限值为:
1.308mg/day÷300mg/day=0.436%
2类杂质根据TTC的计算方法,即药物若用于长期治疗(>10年),则杂质按TTC的可接受摄入量计算限值。若药物用于短期治疗,则杂质的可接受摄入量参考表1进行调整,再结合其它因素制定合适的限值。
例3.根据TTC可接受摄入量计算限值
某C药中含2类杂质c,C药临床用量为:1.5mg/day,每3天增加0.5~1mg,成人最大给药量为20mg/day,疗程不超过3~6个月。
按终生给药的TTC可接受摄入量为1.5μg/day,但根据该药6个月的给药周期,杂质c每日最大可接受摄入量调整为20μg/day。
C药的每日最大临床剂量为20mg/day,则杂质c的限值为20μg/day÷20mg/day=0.1%
3类杂质经(Q)SAR方法测试确定为3类的杂质,可进行细菌回复突变试验,若试验结果显示有致突变性,则杂质归为2类,根据TTC的计算方法制定限值。若试验结果显示无致突变性,则杂质归为5类,按5类杂质制定限值。如果长期给药时杂质日摄入量超出1mg,或杂质的水平不能被控制在一个适当的可接受水平,则可以进行体内基因突变试验,以了解体内基因突变试验与细菌回复突变试验结果的相关性,也可选择其它体内遗传毒性试验,根据适当的体内测试结果可以制定化合物特定杂质的限值。如未进行细菌回复突变试验则采用与2类杂质相同的根据TTC的计算方法制定限值。
4类和5类杂质按非致突变杂质进行限值控制。



