

NEWS CENTER
新闻中心
原辅料相容性试验指导原则
来源:英格尔医药 发布时间:2020-05-14
原辅材料相容性实验在药物研发环节中极为关键,为处方中辅助材料的选取提供了非常有益的数据和参考资料。辅助材料的各项性质,还有外界多种要素都有可能影响到原辅材料相容性,在药物研发的早期就须要开展考察。法规对各类剂型的原辅材料相容性考察进行了强制的规定,只是并沒有提供详尽的实验实际操作细节,这须要大家遵从科学的原则,开展合理的实验设计。在做原辅材料相容性实验时,大家现在首要关注原辅材料化学反应造成形状改变,药物含量减少和杂质上升等,而在实际操作环节中,辅助材料的吸附还有原辅材料形成复合物等其它复杂情况也可能影响到药品质量,应该给予注意。
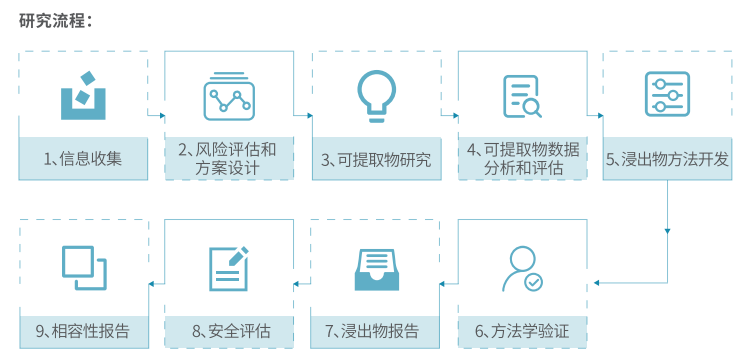
原辅材料相容性实验的标准操作流程

恒温恒湿箱或通过在密闭容器下部放置饱和盐溶液来实现。依据不同的环境湿度要求,选取NaCl饱和溶液(15.5-60℃,RH75%±14%)或KNO3饱和溶液(25℃,RH92.5%)。
光照实验
供试品置光照箱或其它适宜的光照容器内,于照度4500Lx±500Lx条件下放置10天,在第5天和第10天取样检测。
上述为影响因素稳定性研究的一般的要求。依据药品的性质必要时还可以设计构思其他实验,如考察pH值、氧、低温、冻融等因素对药品稳定性的影响到。
4.2原辅材料相容性实验-针对国外申报项目
选取辅助材料:>2个辅助材料每一类功能性辅助材料(例如:填充剂、粘合剂、崩解剂、润滑剂、润湿剂、助流剂、包衣材料);
API和辅助材料的配比:接近处方中的常用配比
API1:10
API:粘合剂或崩解剂:1:1
API:润滑剂或助流剂:10:1
容器/封装:管/密封,500mg粉末/管
贮存条件:加速40℃/75%RH开口,50℃/75%RH/密闭
取样时间:0天,2周,4周
药物样品分析:物理外观,含量和杂质(含量和杂质必须来自同一药物样品)其他注意事项:
1:在各类实验条件下需设计构思API的参比并检验
2:还可以准备第二份药物样品粉末混合物加5%的水,双工作负荷
3:硬脂酸和磷酸氢钙在40℃
原辅材料相容实验,从药物研发者的角度来看,为药物辅助材料和药物工艺的选取确定提供合理有效的数据。从监管者的角度来看,提供原辅材料相容实验数据,是评价辅助材料是否影响到产品质量的关键考虑。从国内外药品监管机构的相关要求检索还可以发现,对原辅材料相容实验实际操作并沒有开展过多的具体规定,因此,研究人员应该依据各个品种的特点设计构思实验的条件和方式,研究设计得合理、科学即可,最关键的是研究者能够获得有效和有价值的信息。
上一篇原辅料相容性实验
下一篇药物原辅料相容性试验



